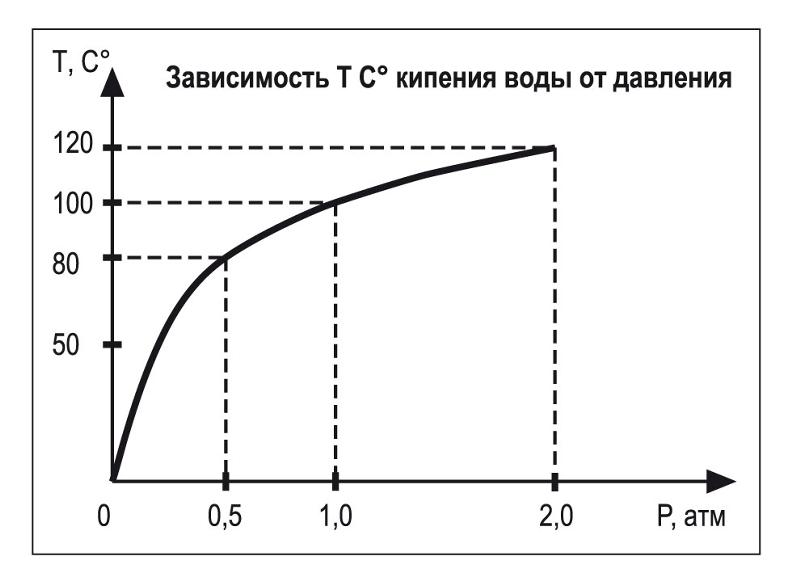
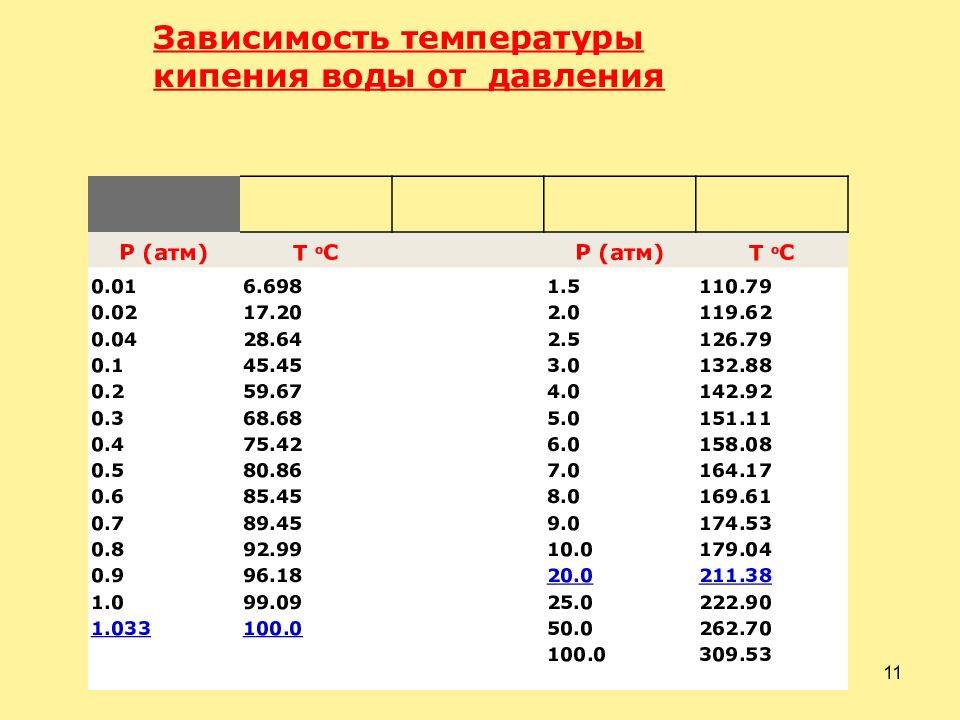
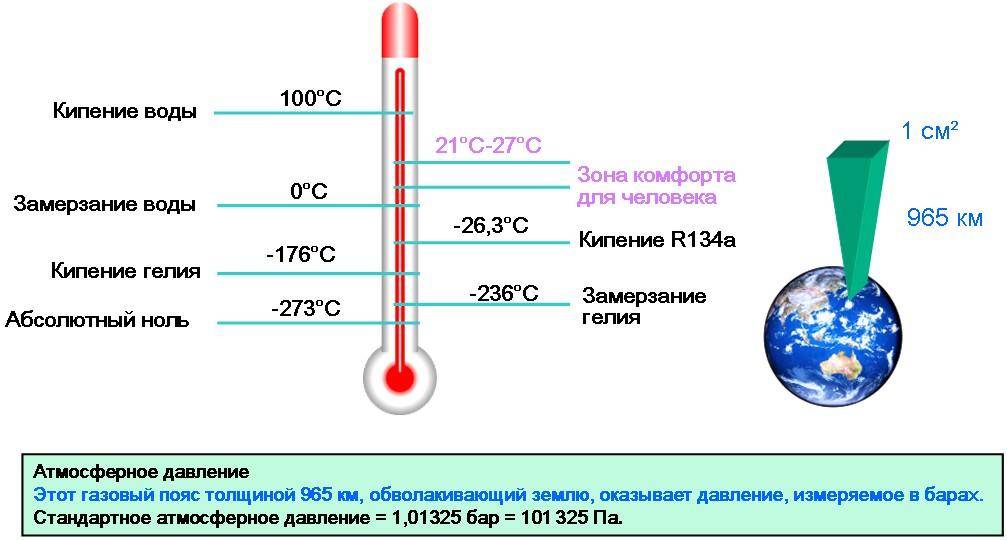
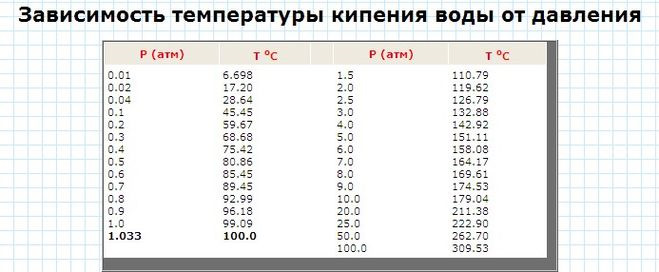
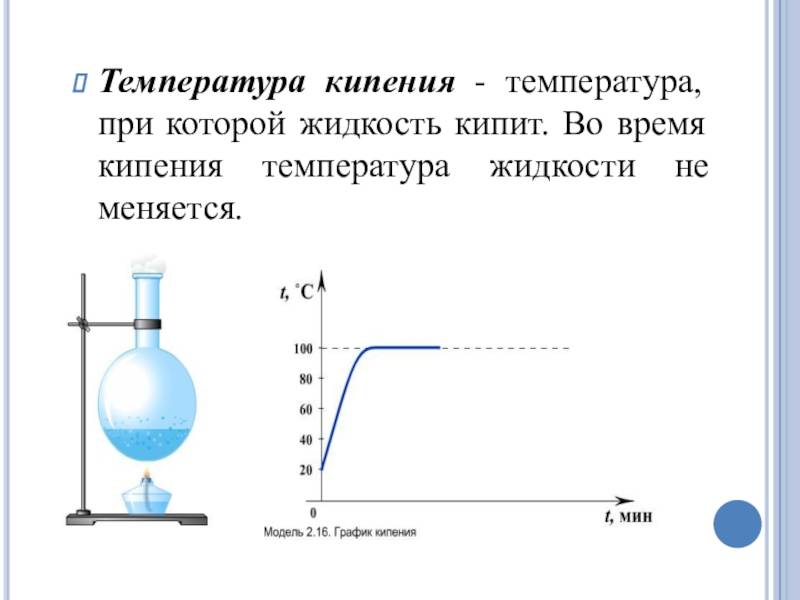
Как происходит процесс кипения воды?
Кипение воды является сложным процессом, который происходит в четыре стадии. Рассмотрим пример кипения воды в открытом стеклянном сосуде.
На первой стадии кипения воды на дне сосуда появляются небольшие пузырьки воздуха, которые также можно заметить и на поверхности воды по бокам.
Эти пузырьки образуются в результате расширения небольших пузырей воздуха, которые находятся в мелких трещинах сосуда.
На третьей стадии на поверхность воды поднимается огромное количество пузырьков, что вначале вызывает небольшое помутнение воды, которая затем «бледнеет». Данный процесс продолжается недолго и имеет название «кипение белым ключом».
Наконец, на четвертой стадии кипения вода начинает интенсивно бурлить, появляются большие лопающиеся пузыри и брызги (как правило, брызги означают, что вода сильно перекипела).
Из воды начинает образовываться водяной пар, при этом вода издает специфические звуки.
Удельная теплота кипения воды
Удельная теплота кипения воды или парообразования – это физическая величина, отражающая количество теплоты, необходимое для превращения 1 л кипящей воды в пар.
Процесс кипения воды, как и любого другого вещества, происходит с поглощением теплоты. Значительная часть проводимой теплоты необходима для разрыва связей между молекулами воды.
Другая часть теплоты расходуется на процессы, происходящие при расширении пара. В результате поглощения теплоты увеличивается энергия взаимодействия между частицами пара.
Эта энергия становится больше энергии взаимодействия молекул воды. Таким образом, при одинаковой температуре внутренняя энергия пара становится выше внутренней энергии жидкости.
Единица удельной теплоты парообразования в системе СИ: Дж/кг.
Удельная теплота испарения воды равна 2260 кДж/кг.
Небольшое видео — измерение температуры кипения воды:
Литература
- Кипение // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Исаченко В. П., Осипова В. А., Сукомел А. С. Теплопередача. — М.: Энергия, 1969.
- Кикоин И. К., Кикоин А. К. Молекулярная физика. — М., 1963.
- Радченко И. В. Молекулярная физика. — М., 1965.
- Михеев М. А. Глава 5 // Основы теплопередачи. — 3-е изд. — М.—Л., 1956.
- Петухов Б. С., Генин Л. Г., Ковалев С. А. Теплообмен в ядерных энергетических реакторах. — М.: Энергоатомиздат, 1986.
- Кириллов П. Л., Юрьев Ю. С., Бобков В. П. Справочник по теплогидравлическим расчетам. — М.: Энергоатомиздат, 1990.
- Кипение // : / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
Будет ли спирт кипеть в вакууме?
Спирт — это название гидроксильной группы, данное углеродным соединениям, оканчивающимся на -ОН. В общих случаях этанол, который является наиболее часто используемым соединением из группы спиртов, обычно называют спиртом.
Поэтому, когда мы рассматриваем спирт в условиях вакуума, мы имеем в виду этанол в условиях вакуума. Как уже говорилось в предыдущем разделе, этанол кипит быстрее в условиях вакуума, чем в условиях окружающей среды. Это связано с тем, что давление окружающей среды снижается. При нормальных атмосферных условиях этанол кипит при 76 градусах Цельсия, а в условиях вакуума быстрее кипит при 38 градусах Цельсия.
Водно-спиртовой раствор
Дело в том, что водка не является чистым спиртом, а представляет собой раствор воды, в котором присутствует доля спирта. В зависимости от того, какова эта доля, меняется температура замерзания.
«Разброс» значений, при которых водка подвергается кристаллизации, от -27ºС до -34ºС. Это приблизительные показатели. Чем больше этанола в водке, тем ниже будет предел, когда она сможет превратиться из жидкого алкоголя в, так сказать, «алкогольное мороженое».
Интересно следующее: процесс замерзания идет постепенно, водка загустевает, превращаясь в подобие желе, и только после этого, если температура не меняется, становится твердой. И целиком она почти никогда не замерзает.
Причина: сначала меняют свои характеристики частички воды — они становятся маленькими льдинками. Концентрация спирта в бутылке становится выше, поэтому теперь раствору требуется более низкая температура, чтобы он стал льдом.
Вряд ли в холодильнике возможно создание условий, когда градус понизится до -33 или -40. Это в быту просто технически невозможно, даже если морозильная установка исправна. Поэтому полное превращение в лед вам вряд ли доведется наблюдать, а вот куски льда в бутылке – это вполне вероятно.
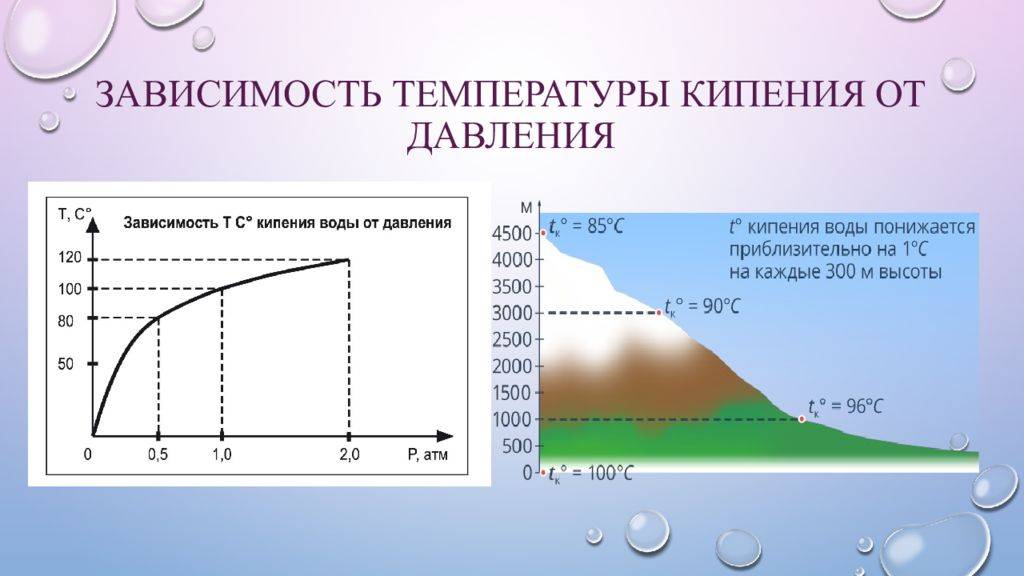
Кипение жидкостей. Зависимость температуры кипения от давления
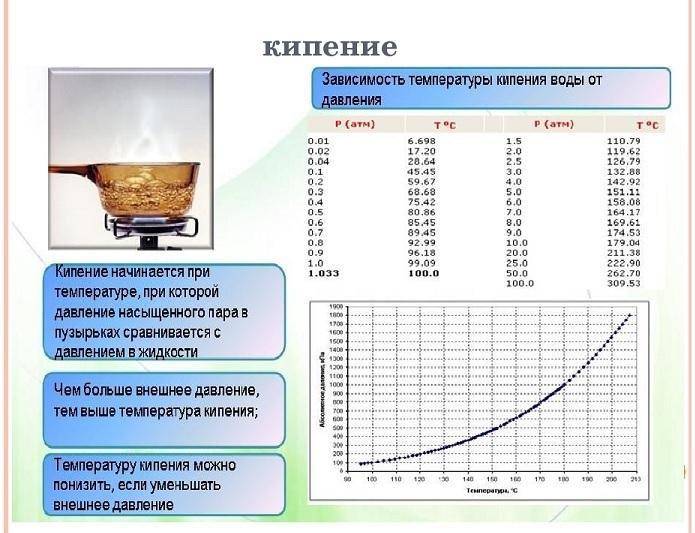
Кипение — это парообразование, происходящее одновременно и с поверхности, и по всему объему жидкости. Оно состоит в том, что всплывают и лопаются многочисленные пузырьки, вызывая характерное бурление.
Как показывает опыт, кипение жидкости при заданном внешнем давлении начинается при вполне определенной и не изменяющейся в процессе кипения температуре и может происходить только при подводе энергии извне в результате теплообмена (рис. 1):
где L — удельная теплота парообразования при температуре кипения.
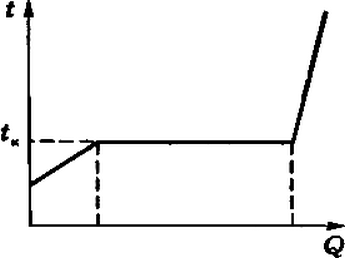
Рис. 1
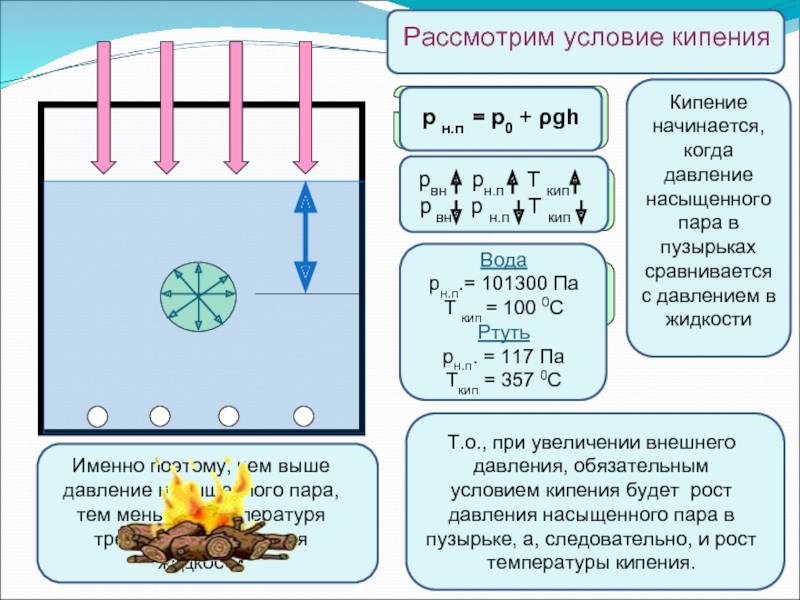
Механизм кипения: в жидкости всегда имеется растворенный газ, степень растворения которого понижается с ростом температуры. Кроме того, на стенках сосуда имеется адсорбированный газ. При нагревании жидкости снизу (рис. 2) газ начинает выделяться в виде пузырьков у стенок сосуда. В эти пузырьки происходит испарение жидкости. Поэтому в них, кроме воздуха, находится насыщенный пар, давление которого с ростом температуры быстро увеличивается, и пузырьки растут в объеме, а следовательно, увеличиваются действующие на них силы Архимеда. Когда выталкивающая сила станет больше силы тяжести пузырька, он начинает всплывать. Но пока жидкость не будет равномерно прогрета, по мере всплытия объем пузырька уменьшается (давление насыщенного пара уменьшается с понижением температуры) и, не достигнув свободной поверхности, пузырьки исчезают (захлопываются) (рис. 2, а), вот почему мы слышим характерный шум перед закипанием. Когда температура жидкости выравняется, объем пузырька при подъеме будет возрастать, так как давление насыщенного пара не изменяется, а внешнее давление на пузырек, представляющее собой сумму гидростатического давления жидкости, находящейся над пузырьком, и атмосферного, уменьшается. Пузырек достигает свободной поверхности жидкости, лопается, и насыщенный пар выходит наружу (рис. 2, б) — жидкость закипает. Давление насыщенного пара при этом в пузырьках практически равно внешнему давлению.
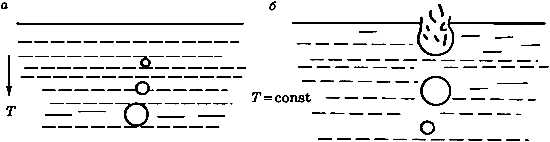
Рис. 2
Температура, при которой давление насыщенного пара жидкости равно внешнему давлению на ее свободную поверхность, называется температурой кипения жидкости.
Так как давление насыщенного пара увеличивается с ростом температуры, а при кипении оно должно быть равно внешнему, то при увеличении внешнего давления температура кипения увеличивается.
Температура кипения зависит также от наличия примесей, обычно увеличиваясь с ростом концентрации примесей.
Если предварительно освободить жидкость от растворенного в ней газа, то ее можно перегреть, т.е. нагреть выше температуры кипения. Это неустойчивое состояние жидкости. Достаточно небольших сотрясений и жидкость закипает, а ее температура сразу понижается до температуры кипения.
Как кипит H2O в таких условиях?
В любом сосуде, заполненном водой, всегда присутствуют частички воздуха. Они остаются на микроскопических трещинах, имеющихся на стенках емкости. По мере нагрева пузырьки увеличиваются, и становятся видимыми невооруженным взглядом, особенно на стенках сосуда и его дне. По сути, это капли насыщенного пара, растворенные в воде.
На определенном этапе пузырьки под действием силы Архимеда начинают выталкиваться наружу. Вода бурлит, но еще не кипит. Это связано с тем, что нагрев происходит неравномерно.
Когда температура на дне сосуда уже достигла 100 °C, а на поверхности воды ещё нет, сила поверхностного натяжения и атмосферное давление препятствуют выходу частиц за пределы емкости. Они возвращаются назад, теряя температуру.
Когда степень нагрева поверхностного и придонного слоя выравнивается, вещество закипает. В вакууме частицам легче покинуть объем сосуда. Этому препятствует только поверхностное натяжение, поэтому кипение начинается при более низкой температуре.
Как будет меняться температура кипения воды: 4 фактора
Температура, при которой кипит жидкость, называется температурой кипения.

Стоит отметить, что она всегда остается неизменной. Поэтому, если увеличить огонь под кипящей кастрюлей с водой, выкипать будет быстрее, но температура при этом не увеличится, так как средняя кинетическая энергия молекул остаётся неизменной.
Рассмотрим 4 фактора, которые влияют на изменение t°:
- Пониженное атмосферное давление (наблюдается в горной местности) – t° уменьшается.
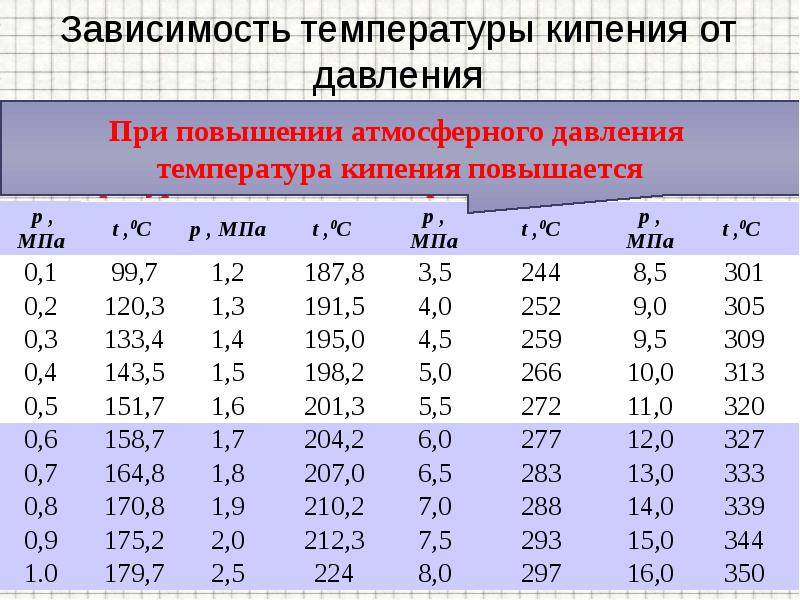
- Повышенное атмосферное давление (наблюдается в шахте) – t° наоборот увеличивается.
- Применения герметической крышки, вакуума. За счёт герметической крышки или посуды пар не выходит градус кипения увеличивается. При использовании вакуума температура зависит от давления, которое создано внутри его.
- Свойства воды. Соленая вода начинает кипеть при более высокой температуре, чем пресная.
Рассмотрим более подробно каждый из факторов.
Влияние атмосферного давления
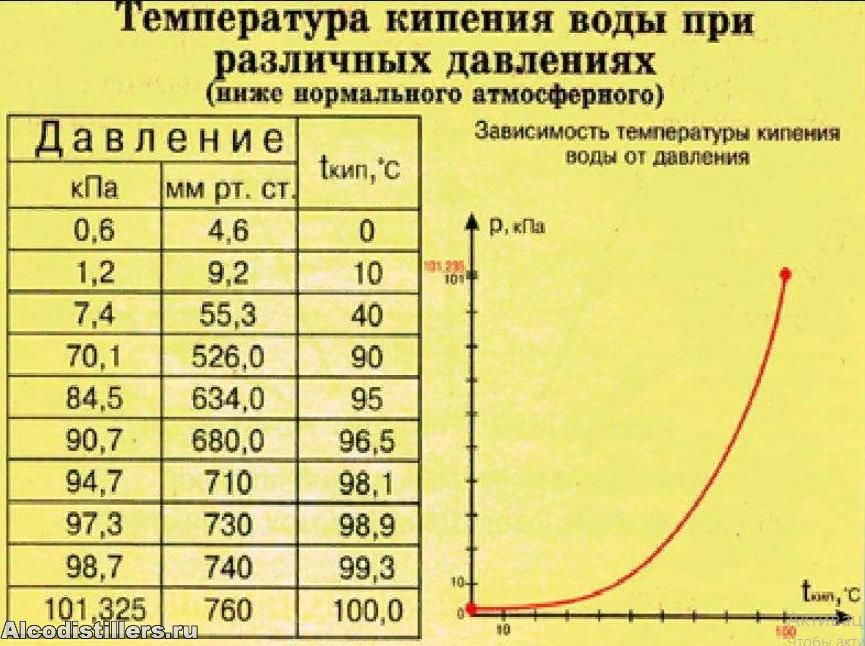
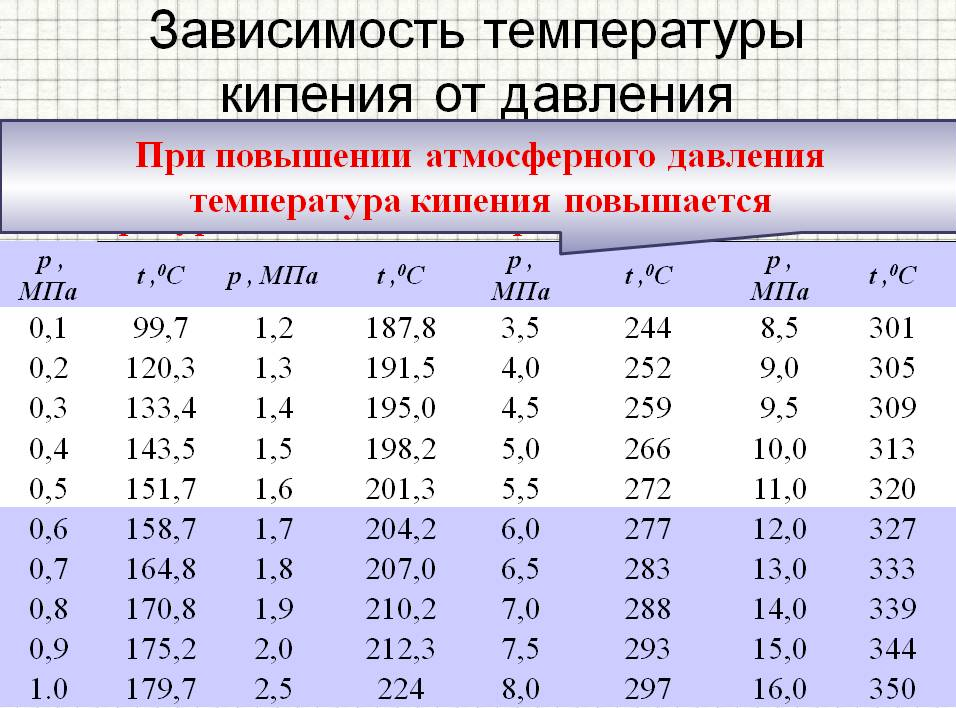
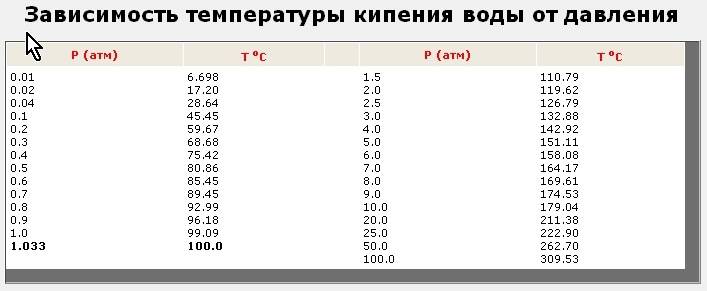
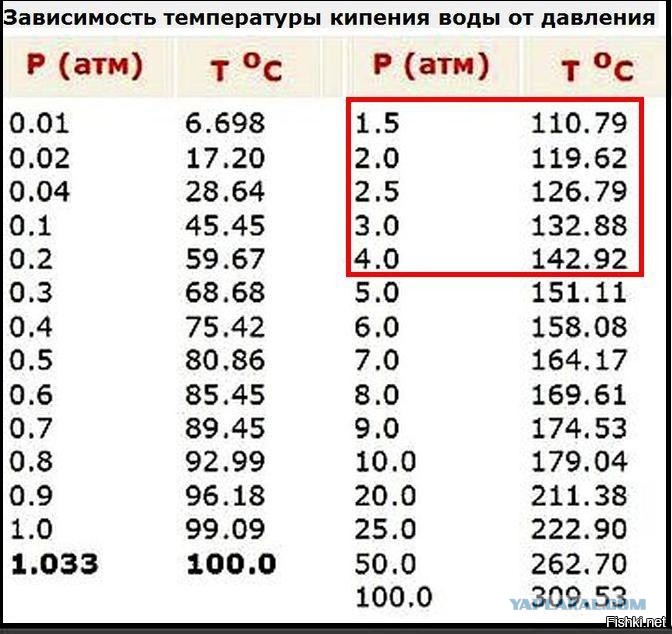
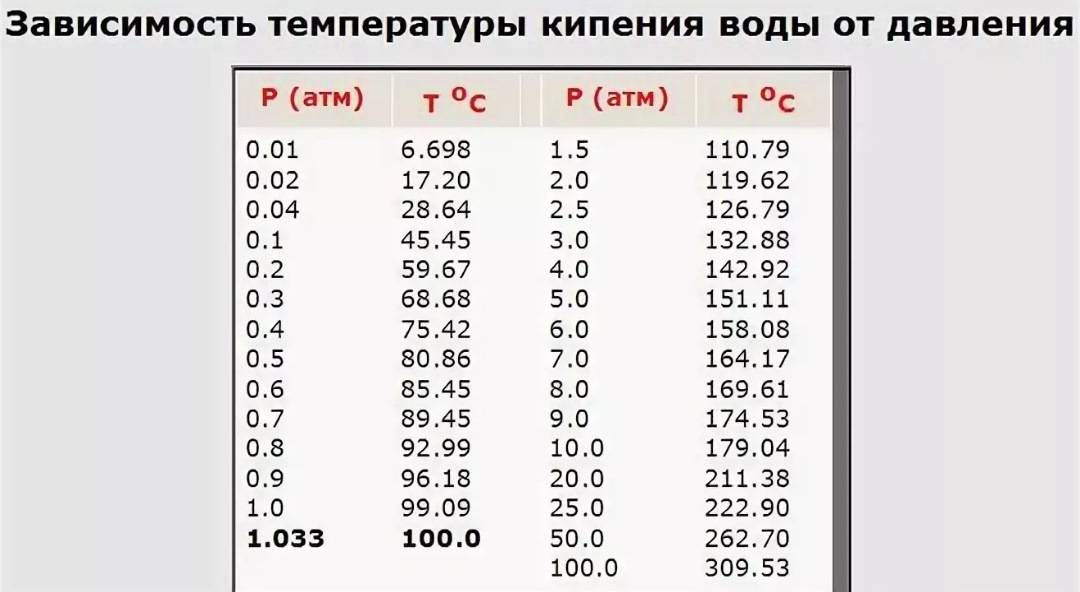
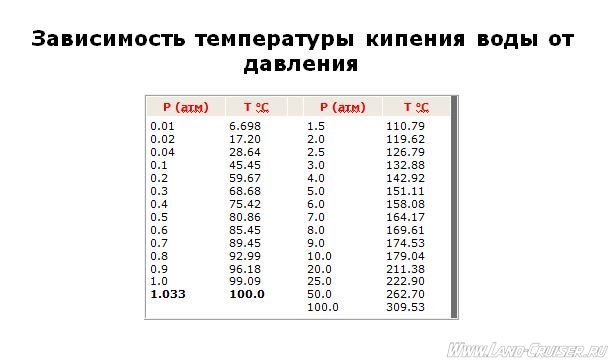
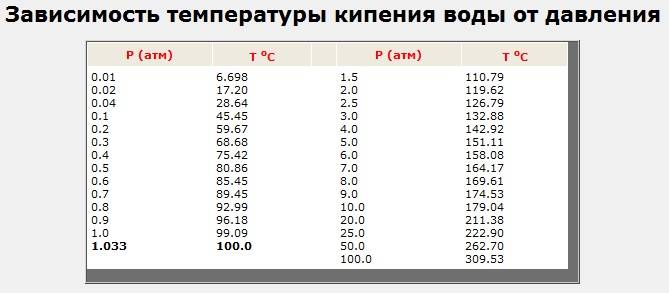
Согласно исследованиям и уравнению Клапейрона — Клаузиуса, градус кипения напрямую зависит от атмосферного давления. С его ростом температура кипения увеличивается, а с уменьшением, наоборот, становится все ниже и ниже.
Атмосферное давление — это давление атмосферы, действующее на все находящиеся на ней предметы и земную поверхность. Оно может меняться в зависимости от места и времени и измеряется барометром.
Таблица № 1. «Температура кипения воды от давления».
| Р, кПа | t, °C | Р, кПа | t, °C | Р, кПа | t, °C |
| 5,0 | 32,88 | 91,5 | 97,17 | 101,325 | 100,00 |
| 10,0 | 45,82 | 92,0 | 97,32 | 101,5 | 100,05 |
| 15,0 | 53,98 | 92,5 | 97,47 | 102,0 | 100,19 |
| 20,0 | 60,07 | 93,0 | 97,62 | 102,5 | 100,32 |
| 25,0 | 64,98 | 93,5 | 97,76 | 103,0 | 100,46 |
| 30,0 | 69,11 | 94,0 | 97,91 | 103,5 | 100,60 |
| 35,0 | 72,70 | 94,5 | 98,06 | 104,0 | 100,73 |
| 40,0 | 75,88 | 95,0 | 98,21 | 104,5 | 100,87 |
| 45,0 | 78,74 | 95,5 | 98,35 | 105,0 | 101,00 |
| 50,0 | 81,34 | 96,0 | 98,50 | 105,5 | 101,14 |
| 55,0 | 83,73 | 96,5 | 98,64 | 106,0 | 101,27 |
| 60,0 | 85,95 | 97,0 | 98,78 | 106,5 | 101,40 |
| 65,0 | 88,02 | 97,5 | 98,93 | 107,0 | 101,54 |
| 70,0 | 89,96 | 98,0 | 99,07 | 107,5 | 101,67 |
| 75,0 | 91,78 | 98,5 | 99,21 | 108,0 | 101,80 |
| 80,0 | 93,51 | 99,0 | 99,35 | 108,5 | 101,93 |
| 85,0 | 95, 15 | 99,5 | 99,49 | 109,0 | 102,06 |
| 90,0 | 96,71 | 100,0 | 99,63 | 109,5 | 102,19 |
| 90,5 | 96,87 | 100,5 | 99,77 | 110,0 | 102,32 |
| 91,0 | 97, 02 | 101,0 | 99,91 | 115,0 | 103,59 |
Единицы измерения давления в таблице: кПа.
Нормальное атмосферное давление составляет 765 мм. РТ. Ст. = 101,325 Р, кПа
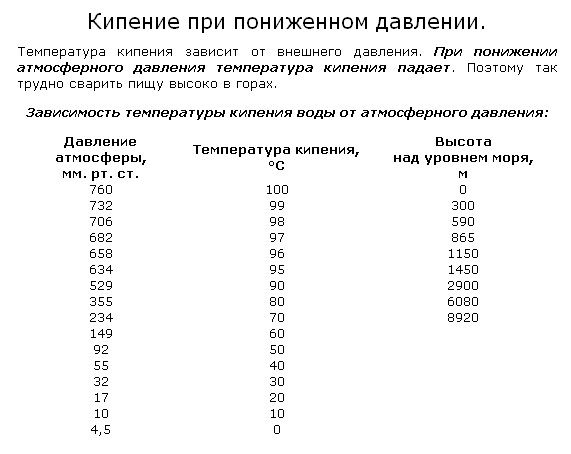
Температура кипения в горах
При подъеме над поверхностью Земли (в горах), температура кипения воды падает, так как снижается атмосферное давление (на каждые 10, 5 м на 1 мм РТ. С). Пузырькам легче всплывать – процесс происходит быстрее.

Для варки мяса, как и других продуктов, нужны привычные 100 градусов. В обратном случае все компоненты бульона просто останутся сырыми.
Таблица № 2. «Как будет меняться t° кипения с высотой».
| Высота над уровнем моря | t° кипения |
| 100,0 | |
| 500 | 98,3 |
| 1000 | 96,7 |
| 1500 | 95,0 |
| 2000 | 93, 3 |
| 2500 | 91,7 |
| 3000 | 90,0 |
| 3500 | 88,3 |
| 4000 | 86,7 |
| 4500 | 85,0 |
| 5000 | 83,3 |
| 6000 | 80,0 |
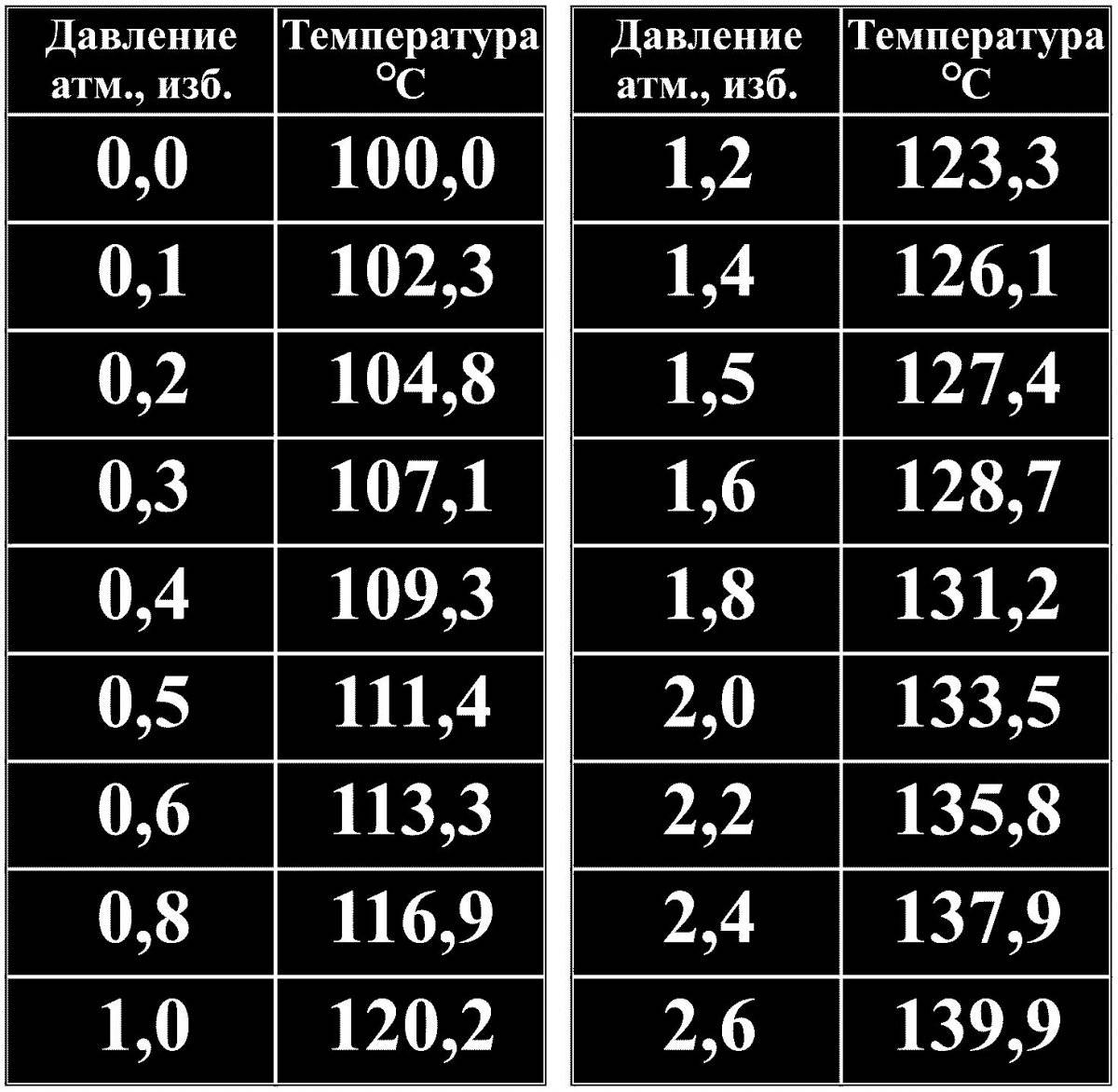
Температура кипения воды в шахте
Если спуститься в шахту, то давление будет увеличиваться.
Температура кипения воды в шахте зависит от глубины (при спуске на 300 м вода закипит при t 101°C, при глубине 600 метров -102 °C
Применение герметической крышки
Герметичные крышки не позволяет образовавшемуся пару ускользнуть. В среднем температура закипания воды увеличивается от 5-20 градусов.
В хозяйстве для приготовления блюд часто используют кастрюли, сковородки с герметичной крышкой. Таким образом, уменьшается время приготовления пищи за счет высокой температуры, а блюда получаются более вкусными. В горных районах с низким давлением это необходимая вещь для приготовления пищи. Так же используют мультиварки и сотейники.
Кипячение воды в вакууме
Вакуум — это среда с газом, с пониженным давлением.
Виды вакуумов:
- низкий;
- средний;
- высокий;
- сверхвысокий;
- экстремальный;
- космическое пространство;
- абсолютный.
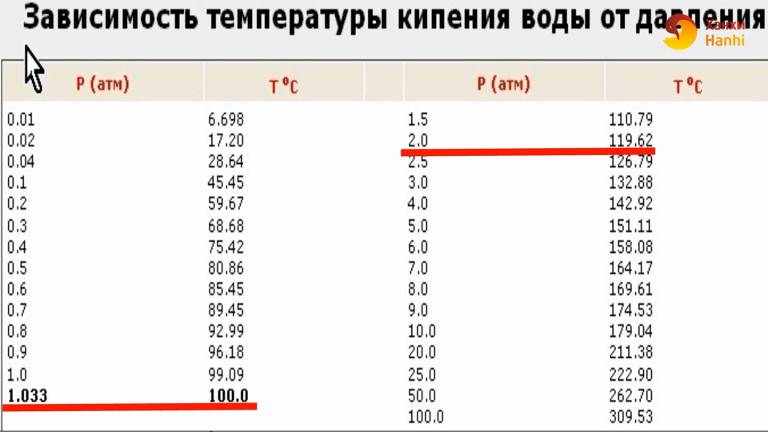
Температура кипения воды в вакууме зависит от того, какое давление в нём.
Кипение солёной воды
Солёная вода закипает при более высокой температуре за счет своих свойств.
Соль увеличивает плотность воды, соответственно на процесс требуется больше времени.
t° повышается примерно на 1 градус при добавлении 40 грамм соли на литр воды.
Температура кипения воды в чайнике
Чистая пресная вода закипает в чайнике при t° 100 градусов °C при условиях нормального атм. давления 760 мм ртутного столба.
Кинетическая энергия
Кинетическая энергия нагретого водяного пара активно используется в промышленности. В частности, на основе энергии пара работает такое устройство как паровая турбина. Она представляет собой насаженный на вал массивный диск, на котором закреплены лопасти. На эти лопасти поступает пар, нагретый в паровом котле и имеющий температуру около 600 градусов. Этот пар расширяется в сопло, происходит превращение его внутренней энергии в кинетическую энергию направленного движения. Струя пара, обладающая большой кинетической энергией поступает из сопло на лопасти турбины, приводя турбину во вращение.
Что считать вакуумом?
 Слово «вакуум» означает абсолютную пустоту, или пространство, свободное от вещества. Когда нет вещества, нечему и кипеть.
Слово «вакуум» означает абсолютную пустоту, или пространство, свободное от вещества. Когда нет вещества, нечему и кипеть.
В науке и технике под ним понимают пространство, где давление значительно ниже атмосферного.
Критерием глубины вакуума является степень разрежения. Она определяется отношением давления в объеме к величине атмосферного. Единица измерения, принятая международной системой мер – Паскаль, но применяются и другие.
Нормальное атмосферное давление, измеренное на уровне моря, принято равным 760 мм ртутного столба, или 101325 Па. Например, разрежение, при котором давление равно 100 Па, считается низким, 0,00001 Па – высоким.
Суть процесса
Прежде всего надо определиться с понятием кипения. Что это такое? Это процесс, при котором вещество превращается в пар. Причем процесс этот происходит не только на поверхности, но и по всему объему вещества.
При кипении начинают образовываться пузырьки, внутри которых находится воздух и насыщенный пар. Шум закипающего чайника, кастрюли указывает на то, что пузырьки воздуха начали всплывать, затем опускаться и лопаться. Когда емкость хорошо прогреется со всех сторон, шум прекратится, значит, жидкость полностью закипела.

Процесс проходит при определенной температуре и давлении и является с точки зрения физики фазовым переходом первого рода.
В таблицах температура кипения воды или другой жидкости при нормальном атмосферном давлении приводится как одна из основных физических характеристик. Температура кипения (Тк) на самом деле равняется температуре пара, который находится в насыщенном состоянии прямо на границе между водой и воздухом. Сама вода, если быть точным, нагрета чуть-чуть больше.

На процесс кипения также ощутимо влияют:
- наличие в воде примесей газа,
- звуковые волны,
- ионизация.

Есть и другие факторы, заставляющие образовываться пузырьки быстрее или медленнее. Следует также отметить, что у каждых веществ своя Тк. Бытует мнение, что если добавить в воду соль, то она закипит быстрее. Это действительно так, но время изменится совсем немного. Для ощутимых результатов придется добавить очень много соли, что полностью испортит блюдо.
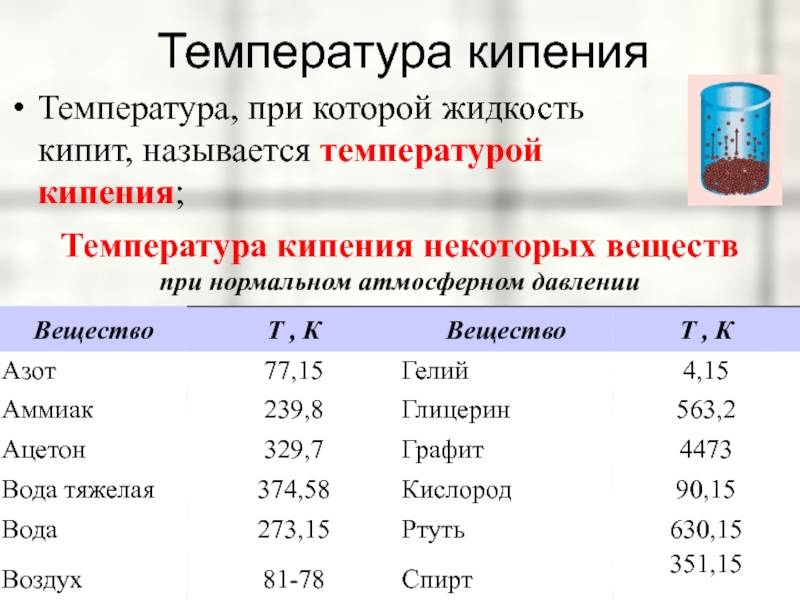
Температура кипения некоторых веществ
В таблице 1 представлены экспериментально полученные значения температуры кипения для различных веществ.
| Вещество | $t_{кип}, \degree C$ | Вещество | $t_{кип}, \degree C$ |
| Водород | -253 | Вода | 100 |
| Кислород | -183 | Ртуть | 357 |
| Эфир | 35 | Свинец | 1740 |
| Спирт | 78 | Медь | 2567 |
| Молоко | 100 | Железо | 2750 |
Талица 1. Температура кипения некоторых веществ (при нормальном атмосферном давлении)
{"questions":[{"content":"Какая температура кипения у свинца?<br />`input-1` $\\degree C$.","widgets":{"input-1":{"type":"input","inline":1,"answer":"1740"}}}]}В обычных условиях кислород является газом. Из таблицы мы видим, что его температура кипения равна $-183 \degree C$. При температуре ниже этой кислород будет жидким.
С другой стороны, вещества, которые мы обычно наблюдаем в твердом состоянии, имеют очень высокую температуру кипения. Например железо плавится и превращается в жидкость при температуре $1539 \degree C$. А чтобы заставить жидкое железо кипеть, необходимо довести его температуры в $2750 \degree C$.
Температура кипения воды в горах
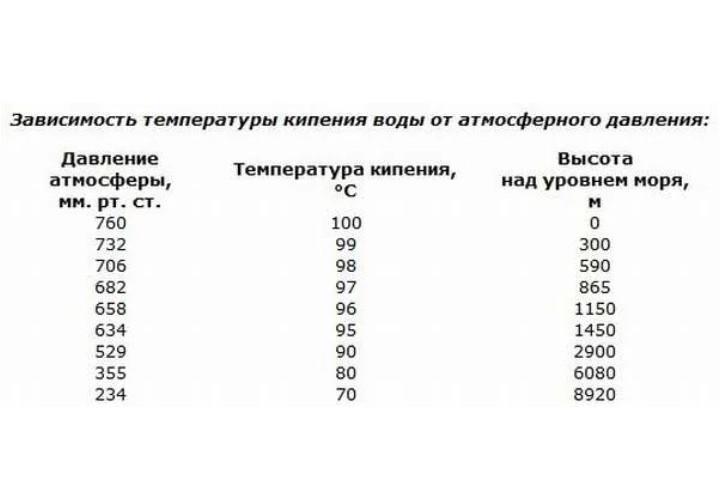
Как уже упоминалось выше, величина температуры кипения воды напрямую зависит от внешнего давления. Чем ниже будет атмосферное давление, тем меньше станет показатель температуры кипения.
Известно, что атмосферное давление значительно падает над уровнем моря. Поэтому в горах давление будет намного ниже, чем на уровне моря.
Любой альпинист знает, что в горах сложно заварить чай, поскольку вода недостаточно нагревается. Также в горах требуется больше времени, чтобы сварить пищу.
Поэтому была составлена специальная таблица, отражающая температуру закипания воды в зависимости от высоты.
Графики кипения жидкостей
На рисунке 2 показаны графики зависимости температуры $T$ от времени $t$ трех разных жидкостей: воды, спирта и эфира. Масса жидкостей одинакова, мощности нагревателей идентичны.
Рисунок 2. Графики зависимости температуры от времени воды, спирта и эфира
На рисунке видно, что горизонтальные участки графиков соответствуют процессам кипения. Они параллельны оси времени, температура на них остается постоянной. Чтобы определить, какой график соответствует каждой жидкости, нам нужно обратиться к таблице 1.
Температура кипения первой жидкости равна $35 \degree C$. Значит, график под номером 1 — это график нагревания и кипения эфира.
$70 \degree C$ — температура кипения спирта. Значит, 2 — график нагревания и кипения спирта.
График 3 соответствует воде, ведь ее температура кипения равна $100 \degree C$
Обратите внимание, что жидкости не нагреются выше своей температуры кипения. Например, при $100 \degree C$ вода полностью перейдет в пар
Пар же может иметь более высокую температуру.
Почему может кипеть при отрицательных температурных значениях?
Когда среда разрежена, вода закипает раньше. Кипение начнется, как только разрежение достигнет величины, при которой температура кипения становится меньше температуры окружающей среды.
Ниже в таблице приведены округленные данные зависимости температуры кипения от давления.
| Давление, Pa | Температура кипения воды | ||
| °C | °F | °K | |
| 101 325 | 100 | 212 | 373 |
| 84 660 | 95 | 205 | 368 |
| 70 060 | 90 | 194 | 363 |
| 47 340 | 80 | 176 | 353 |
| 31 550 | 70 | 158 | 343 |
| 19 900 | 60 | 140 | 333 |
| 12 300 | 50 | 122 | 323 |
| 7 350 | 40 | 104 | 313 |
| 4 230 | 30 | 86 | 303 |
| 3 380 | 27 | 80 | 300 |
| 3 048 | 25 | 76 | 298 |
| 2 710 | 22 | 72 | 295 |
| 2 370 | 20 | 69 | 293 |
| 2 030 | 18 | 64 | 291 |
| 1 670 | 15 | 59 | 288 |
| 1 350 | 12 | 53 | 285 |
| 1 010 | 7 | 45 | 280 |
| 605 | 32 | 273 | |
| 340 | -6 | 21 | 267 |
| 170 | -15 | 6 | 258 |
| 35 | -31 | -24 | 242 |
| 0,16 | -47 | -35 | 226 |
| 0,3 | -51 | -60 | 222 |
| 0,03 | -56 | -70 | 217 |
Вода, отдавая пар, остывает. Он конденсируется и возвращается обратно в жидкое состояние. При дальнейшей откачке воздуха разрежение становится таким, что H2O мгновенно вскипает.
Температура понижается до отрицательной, водяной пар кристаллизуется, образуя лед. Поскольку это сопровождается увеличением объема, образованию льда препятствует внешнее давление.
Чем оно меньше, тем раньше образуется лед. Поэтому, даже при низком разрежении вода неизбежно превратится в пар, затем в лед.
Как это работает
На самом деле космос не холоден, потому что температура является мерой движения молекул. Если у вас нет материи, как в вакууме, у вас нет температуры. Тепло, передаваемое стакану с водой, будет зависеть от того, находится ли он на солнечном свете, в контакте с другой поверхностью или на открытом воздухе в темноте. В глубоком космосе температура объекта будет около -460 ° F или 3K, что очень холодно. С другой стороны, полированный алюминий при ярком солнечном свете, как известно, достигает 850 ° F. Это большая разница температур!
Однако это не имеет большого значения, когда давление почти вакуумное. Подумайте о воде на Земле. На вершине горы вода закипает быстрее, чем на уровне моря. Фактически, в некоторых горах можно выпить чашку кипятка и не обжечься! В лаборатории вы можете заставить воду закипеть при комнатной температуре, просто применив к ней частичный вакуум. Это то, что вы ожидаете от космоса.
См. Кипячение воды при комнатной температуре
Хотя непрактично посещать космос, чтобы увидеть, как вода закипает, вы можете увидеть эффект, не выходя из дома или учебы. Все, что вам нужно, это шприц и вода. Вы можете получить шприц в любой аптеке (игла не требуется) или во многих лабораториях.
- Наберите в шприц небольшое количество воды. Вам просто нужно достаточно, чтобы увидеть это – не наполняйте шприц полностью.
- Положите палец на отверстие шприца, чтобы закрыть его. Если вы боитесь поранить палец, можно прикрыть отверстие куском пластика.
- Наблюдая за водой, как можно быстрее потяните шприц назад. Вы видели, как закипает вода?