Фитохимические вещества для облегчения симптомов аденомы простаты
Фитохимические вещества – растительные соединения, которые обладают защитными или профилактическими свойствами. В последнее время интерес к их использованию для лечения ДГПЖ возобновился и растет. Исследования их эффективности проводятся, однако полученные результаты были неоднозначными, большинство исследований, связанных с фитохимическими веществами, не подвергалось таким же строгим доклиническим фармакологическим испытаниям и крупномасштабным клиническим испытаниям, которые проводятся с альфа-блокаторами и 5-ARI.
Наиболее полно описано и изучено фитотерапевтическое средство Serenoa repens (Сереноа ползучая). Применение этого препарата продемонстрировало эффективность от слабой до умеренной:
- в уменьшении никтурии;
- в увеличении максимального потока мочи;
- улучшении Международной шкалы симптомов простаты (IPSS) у мужчин с ДГПЖ, с результатами, сопоставимыми с эффективностью/результатами тамсулозина.
Однако другие испытания не показали значительного положительного эффекта S. repens по сравнению с плацебо. Проведенный недавно Кокрановский обзор пришел к выводу, что S. repens не более эффективен, чем плацебо для лечения симптомов мочеиспускания при доброкачественной гиперплазии простаты.
Еще одно популярное альтернативное средство лечения аденомы простаты – Pygeum africanum, экстракт африканского чернослива. В Кокрановском обзоре, показано, что его прием обеспечивает умеренное уменьшение проблем с мочеиспусканием, вызванных ДГПЖ. Однако исследования были небольшими, длились недолго, не проверялись различные дозы и препараты, и в большинстве случаев не использовались стандартизованные, проверенные меры оценки эффективности.
Резюме
Итак делаем выводы:
- Перед длительным приемом НПВС обязательным является сбор анамнеза для исключения патологий ЖКТ в прошлом, по необходимости проведение гастроскопии, диагностика и лечение хеликобактериоза.
- Выбирая, чем лечиться, по возможности следует останавливаться на селективных НПВС.
- При назначении неселективных НПВС более 5 дней и у пациентов с эрозивно-язвенными изменениями в анамнезе даже с селективными НПВС обязателен прием препаратов «прикрывающих» желудок (ИПП).
- Всем пациентам в возрастной группе после 60 лет, регулярно принимающим аспирин, обязательно проводить гастроскопию и при высоких рисках принимать постоянно препараты из группы ИПП.
Прием гастроэнтеролога в нашей клинике – 3 900 рублей
Перспективы изучения энзимологии ароматазы и регуляции ее активности
Приведенные в настоящем обзоре данные свидетельствуют о том, что в настоящее время существует значительная база экспериментальных данных по структурной организации, биосинтезу и регуляции активности ароматазы. Исследовано действие поллютантов окружающей среды на ароматазную активность, разработан целый комплекс терапевтических мер, направленных на коррекцию ароматазной активности. Данные о высокоспецифичном и, возможно, необратимом изостерическом ингибировании ароматазы рядом соединений раскрывают новые перспективы в плане поиска природных и неприродных фармакологических агентов, подавляющих ароматазную активность.
Динамическое наблюдение и изменение образа жизни
Динамическое наблюдение – это стратегия управления, во время которой пациент находится под наблюдением врача, но не получает медицинской помощи в виде серьезных лекарств и хирургических методов терапии. Такое бдительное ожидание вместе с изменением образа жизни и периодической переоценкой наиболее подходит пациентам с легкой формой доброкачественной гиперплазии простаты (то есть 7 или менее баллов по результатам анкеты) и/или без каких-либо беспокоящих симптомов, независимо от размера предстательной железы.
Уровень симптоматического дистресса, который пациент может терпеть, значительно варьируется. Поэтому динамическое наблюдение может быть выбором пациента, несмотря на высокий индекс симптомов Американской урологической ассоциации (AUA-SI) или оценку IPSS (напомним, INTERNATIONAL PROSTATE SYMPTOM SCORE или международная оценка симптомов простаты, анкета, которую пациент заполняет во время консультации уролога).
Предлагаются различные изменения образа жизни, включающие:
- ограничение жидкости;
- отказ от раздражающих продуктов или напитков (например, кофеина, алкоголя);
- отказ и/или контроль приема некоторых лекарств (например, мочегонных, противоотечных, антигистаминных, антидепрессантов);
- своевременное мочеиспускание;
- упражнения для тазового дна;
- устранение запоров.
Отказ от спиртного
Личный опыт
Вероятно, у каждого врача есть собственный фармакотерапевтический справочник, отражающий его личный клинический опыт применения препаратов, пристрастия и негативное отношение. Успех применения лекарства у одного-трех-десяти первых пациентов обеспечивает пристрастие к нему врача на многие годы, а литературные данные укрепляют мнение о его эффективности. Привожу список некоторых современных бета-блокаторов, на которые у меня есть свой опыт клинического применения.
Пропранолол
Первый из бета-блокаторов, который я стал применять в своей практике. Кажется, в середине 70‑х годов прошлого века пропранолол был чуть ли не единственным бета-блокатором в мире и уж точно — единственным в СССР. Препарат до сих пор относится к наиболее часто назначаемым среди бета-блокаторов, имеет больше показаний к применению по сравнению с другими бета-блокаторами. Однако, применение его в настоящее время я не могу считать оправданным, т. к. другие бета-блокаторы имеют гораздо менее выраженные побочные эффекты.
Пропранолол можно рекомендовать в комплексной терапии ишемической болезни сердца, он также эффективен для снижения артериального давления при гипертонической болезни. При назначении пропранолола существует риск развития ортостатического коллапса
Пропранолол с осторожностью назначают при сердечной недостаточности, при фракции выброса менее 35 % препарат противопоказан.
По моим наблюдениям, пропранолол эффективен при лечении пролапса митрального клапана: дозировки 20–40 мг в сутки достаточно, чтобы пролабирование створок (обычно передней) исчезло или существенно уменьшилось с третьей-четвертой степени до первой или нулевой.
Бисопролол
Кардиопротективный эффект бета-блокаторов достигается при дозировке, которая обеспечивает ЧСС 50-60 в минуту.
Высокоселективный бета1‑блокатор, в отношении которого было доказано снижение смертности от инфаркта миокарда на 32 %. Доза 10 мг бисопролола эквивалентна 100 мг атенолола, препарат назначается в суточной дозировке от 5 до 20 мг. Бисопролол уверенно можно назначать при сочетании гипертонической болезни (снижает артериальную гипертензию), ишемической болезни сердца (уменьшает потребность миокарда в кислороде, уменьшает частоту приступов стенокардии) и сердечной недостаточности (уменьшает постнагрузку).
Метопролол
Препарат относится к бета1‑кардиоселективным бета-блокаторам. У пациентов с ХОБЛ метопролол в дозе до 150 мг/сутки вызывает менее выраженный бронхоспазм по сравнению с эквивалентными дозами неселективных бета-блокаторов. Бронхоспазм при приеме метопролола эффективно купируется бета2‑адреномиметиками.
Метопролол эффективно снижает частоту желудочковых тахикардий при остром инфаркте миокарда и обладает выраженным кардиопротекторным действием, снижая уровень смертности кардиологических больных в рандомизированных исследованиях на 36 %.
В настоящее время бета-адреноблокаторы следует рассматривать как препараты первой линии при лечении ишемической болезни сердца, гипертонической болезни, сердечной недостаточности. Прекрасная сочетаемость бета-блокаторов с мочегонными, блокаторами кальциевых канальцев, ингибиторами АПФ, несомненно, является дополнительным аргументом при их назначении.
Мифы, с которыми мы сталкиваемся в ежедневной практике
Миф 1. Использование НПВС препаратов в виде свечей является менее агрессивным для желудка, нежели приём таблеток
Это 100% миф. Патогенное, разрушительное действие лекарства реализуется через кровь, доставляющую его по сосудам в желудок.
Миф 2. В качестве «гастропротекторов» можно использовать лекарства из группы антацидов — Ренни, Маалокс, Фосфалюгель и H2-блокаторы (Ранитидин и Фамотидин)
В данном случае они не эффективны.
Миф 3. Принимать ингибиторы протонной помпы можно нерегулярно
Дело в том, что если пожилому человеку назначили на всю жизнь противовоспалительный препарат, абсолютно бессмысленно назначать гастропротекцию на месяц. В подобных случаях лекарства должны приниматься строго параллельно.
Миф 4. В качестве «гастропротекторов» могут выступать пищевые продукты (кисели и пр.)
Этот миф, как абсолютно фантастический, мы оставим без комментариев.
Механизм каталитического действия ароматазы
Биосинтез стероидных гормонов происходит главным образом на микросомах и сводится к реакциям гидроксилирования их стероидных предшественников, приводящим к отщеплению алифатических радикалов и образованию полярных продуктов, а также к дегидрогеназным реакциям, обеспечивающим взаимопревращения гидроксильных и кетогрупп . Реакции гидроксилирования осуществляют изоформы цитохрома Р-450, являющиеся конечным пунктом микросомальной цепи переноса электронов . Акцептируя электроны, изоформы цитохрома Р-450 осуществляют гидроксилирование субстрата. Цепь переноса электронов к каталитическому центру ферментов может включать различные компоненты, на основании чего цитохромы Р-450 делятся на четыре основных класса . Ароматаза является представителем четвертого класса изоформ цитохрома Р-450, акцептирующим электроны от НАДФН+Н+ при участии НАДФН+Н+-зависимой цитохром P-450-pe- дуктазы .
На рис. 4 представлен механизм каталитического гидроксилирования субстрата, являющийся общим для всех изоформ цитохрома Р-450 независимо от состава цепи переноса электронов. Он включает следующие основные этапы . Геминовое железо, находясь в окисленном состоянии (Fe3+), акцептирует один электрон от НАДФН+Н+, приобретая степень окисления Fe2+. Восстановившись, железо передает электрон кислороду, в результате чего последний превращается в супероксидный радикал , способный взаимодействовать с Fe3+ в составе цитохрома Р-450. После связывания Fe3+ с супероксидом образуется неустойчивый комплекс FeOO-, который протонируется с образованием FeOOH. Второй электрон, поставляемый НАДФН+Н+-зависимой цитохром Р-450- редуктазой, разрушает пероксидную связь в составе комплекса FeOOH с образованием радикала FeO* и гидроксил-аниона, акцептирующего протон с образованием воды. Радикал FeO* акцептирует водород от гидроксилируемого участка стероидной молекулы с образованием стероидного радикала и FeOH. Далее образовавшийся стероидный радикал, отнимая гидроксил от геминового железа цитохрома Р-450, превращается в гидроксилированный стероид, а каталитический центр цитохрома Р- 450 готов к приему новых электронов и гидроксилированию следующей молекулы субстрата. Механизм каталитического действия ароматазы, включающий несколько процессов гидроксилирования, идущих по описанной выше схеме, представлен на рис. 5. На схеме отражены пути переноса электронов, протонов и кислорода, а также изменения валентности железа. Данная схема была впервые предложена S. Graham-Lorence и соавт. .
Как это работает?
Как же действуют эти препараты в наших желудках? Всё очень просто, негативное воздействие реализуется за счёт дисбаланса защитных и агрессивных сил. У нас в желудке существует ряд защитных механизмов, позволяющих противостоять натиску агрессоров. Среди последних:
- Кислота, которая по своему pH-балансу приближается к аккумуляторной кислоте
- Желчь и сок поджелудочной железы, которые могут забрасываться в желудок.
- Ряд лекарственных препаратов.
- Алкоголь и никотин.
- Раздражающие пищевые компоненты (специи, острая пища и т.д.)
- Инфекция Helicobacter pylori и так далее.
Защищается желудок за счет мощного слоя слизи и бикарбонатов, которые нейтрализуют кислоту, адекватного кровоснабжения, способности очень быстро регенерировать. Когда мы используем НПВС препараты, баланс сил изменяется в сторону агрессивных механизмов и происходит поражение слизистого и подслизистого слоя желудка и 12-перстной кишки.
Побочные действия
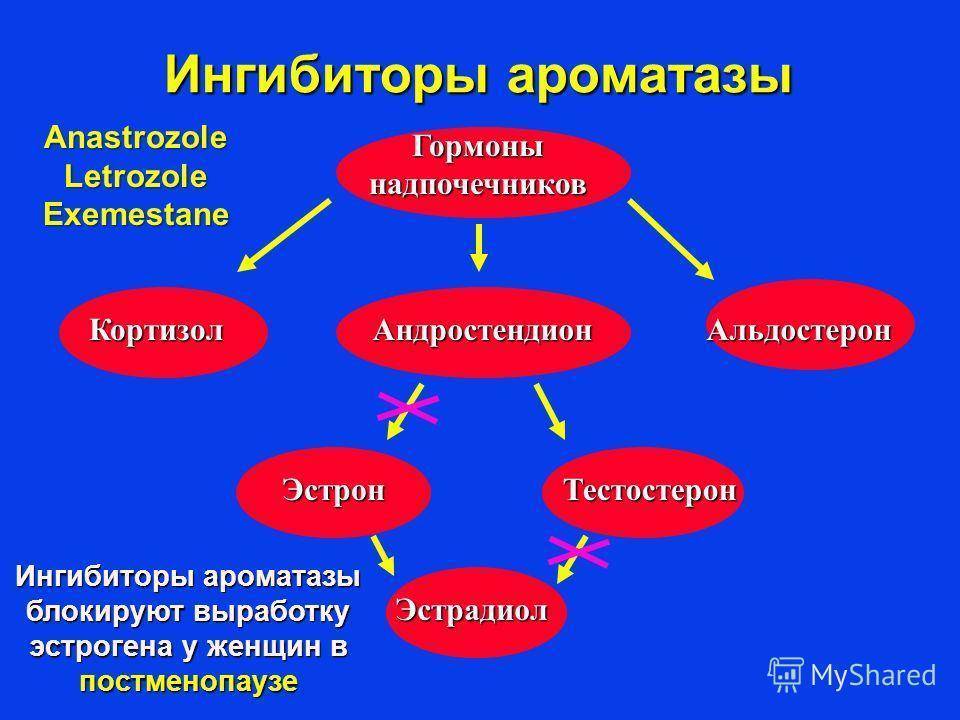
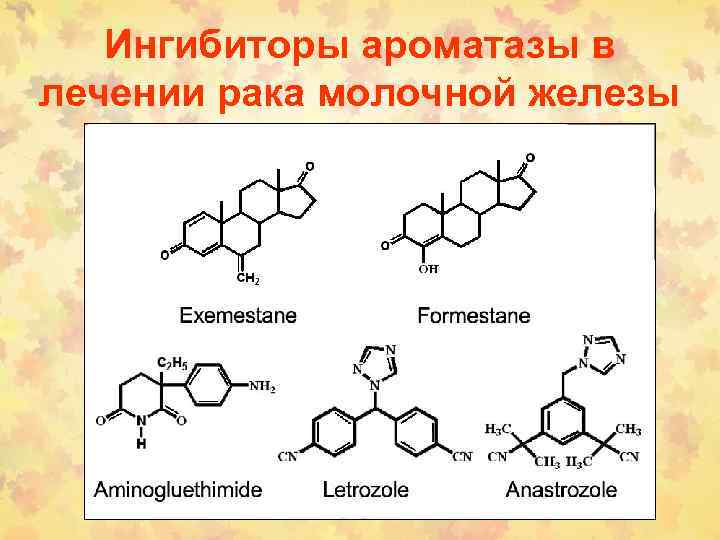
Антиэстрогены и ингибиторы ароматазы обладают схожими побочными реакциями, самые опасные из которых: образование тромбов и дисгормональный остеопороз. Тамоксифен активнее влияет на свертываемость крови, и при многолетнем использовании у небольшого процента женщин индуцирует рак эндометрия. Ингибиторы ароматазы чаще осложняются остеопорозом. Одинаково часто обе группы вызывают приливы.
Все гормональные препараты подвергаются трансформации в печени. Тамоксифен может вызвать токсическое поражение печени и привести к застою желчи — холестазу, клиника которого отчасти напоминает острый холецистит, все симптомы исчезают после отмены антиэстрогена.
В настоящее время нет однозначного мнения по выбору лекарственного средства — эффективность их одинаковая, поэтому ориентируются на гормональный возраст и сопутствующую патологию, к примеру, при варикозной болезни или патологии эндометрия целесообразно избегать тамоксифена, при остеопорозе — ингибиторов.
В подавляющем большинстве случаев ГТ хорошо переносится, что позволяет при неблагоприятных прогностических факторах пролонгировать её до 7-10 лет.
Возможные последствия
На фоне приёма тамоксифена:
- при метастазах в костях рака молочной железы в первый месяц лечения могут усилиться боли — синдром «вспышки» требует отмены антиэстрогена;
- стимулируется овуляция и возможна беременность, поэтому женщины репродуктивного возраста должны прибегать к контрацепции;
- течение кардиальных заболеваний улучшается вследствии благоприятного действия на обмен липидов, но только после нескольких лет ГТ;
- опосредованное повышение в крови эстрогенов приводит к приливам, но также несколько «омолаживает» кожу и слизистые половых органов;
- осложнения со стороны глаз редки, но возможно обострение давней ретинопатии, кератопатии или усугубление возрастной катаракты.
Использование препарата группы ГРГ часто сопровождается посткастрационным синдромом с приливами, частыми кольпитами, недержанием мочи, болями в мочевом пузыре и т.д. У женщин в пременопаузе при совместном применении ГРГ с ингибитором ароматазы возможно повышение уровня эстрадиола, что исключает эффект от лечения.
Бета-адренорецепторы и механизмы действия бета-блокаторов
Различают бета1‑адренорецепторы, находящиеся в основном в сердце, кишечнике, ткани почек, в жировой ткани, ограниченно — в бронхах. Бета2‑адренорецепторы находятся в гладкой мускулатуре сосудов и бронхов, в желудочно-кишечном тракте, в поджелудочной железе, ограниченно — в сердце и коронарных сосудах. Ни одна ткань не содержит исключительно бета1– или беты2‑адренорецепторы. В сердце соотношение бета1– и бета2‑адренорецепторов ориентировочно 7:3.
Таблица 1. Основные показания к применению бета-адреноблокаторов
Механизм действия бета-блокаторов основан на их строении, сходном с катехоламинами. Бета-блокаторы выступают конкурентными антагонистами катехоламинов (адреналина и норадреналина). Терапевтический эффект зависит от соотношения концентрации препарата и катехоламинов в крови.
Блокада бета1‑адренорецепторов приводит к уменьшению ЧСС, сократимости и скорости сокращения сердечной мышцы, при этом снижается потребность миокарда в кислороде.
- Бета-блокаторы вызывают депрессию 4‑й фазы диастолической деполяризации клеток проводящей системы сердца, что обусловливает их антиаритмический эффект. Бета-блокаторы снижают поток импульсов через атриовентрикулярный узел и уменьшают скорость проведения импульсов.
- Бета-блокаторы уменьшают активность ренин-ангиотензиновой системы благодаря уменьшению высвобождения ренина из юкстагломерулярных клеток.
- Бета-блокаторы влияют на симпатическую активность вазоконстрикторных нервов. Назначение бета-блокаторов без внутренней симпатомиметической активности приводит к снижению сердечного выброса, периферическое сопротивление повышается, но приходит к норме при длительном применении.
- Бета-блокаторы ингибируют апоптоз кардиомиоцитов, обусловленный катехоламинами.
- Бета-блокаторы стимулируют эндотелиальную аргинин/нитроксидную систему в клетках эндотелия, т. е. включают основной биохимический механизм расширения сосудистых капилляров.
- Бета-блокаторы блокируют часть кальциевых каналов клеток и снижают содержание кальция в клетках сердечной мышцы. Вероятно, с этим связано снижение силы сердечных сокращений, отрицательный инотропный эффект.
Некардиологические показания к применению бета-блокаторов
- тревожные состояния
- алкогольный делирий
- юкстагломерулярная гиперплазия
- инсулинома
- глаукома
- мигрень (предупреждение приступа)
- нарколепсия
- тиреотоксикоз (лечение нарушений ритма)
- портальная гипертензия
Таблица 2. Свойства бета-адреноблокаторов: полезные и побочные эффекты, противопоказания

Переносимость сартанов
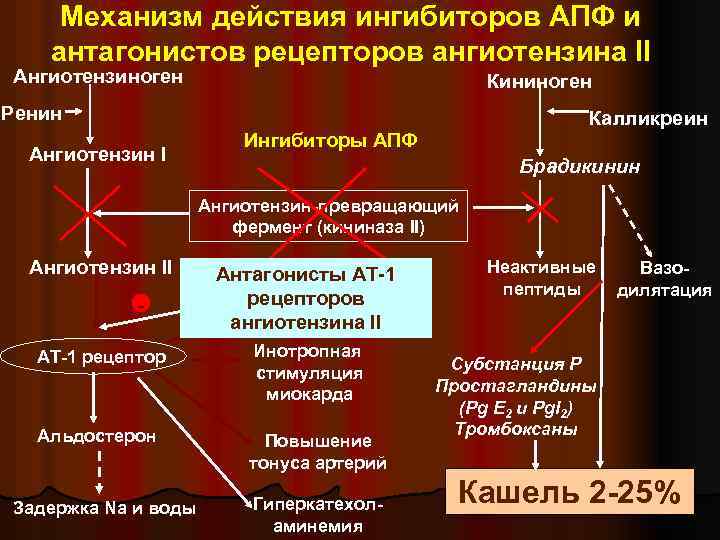
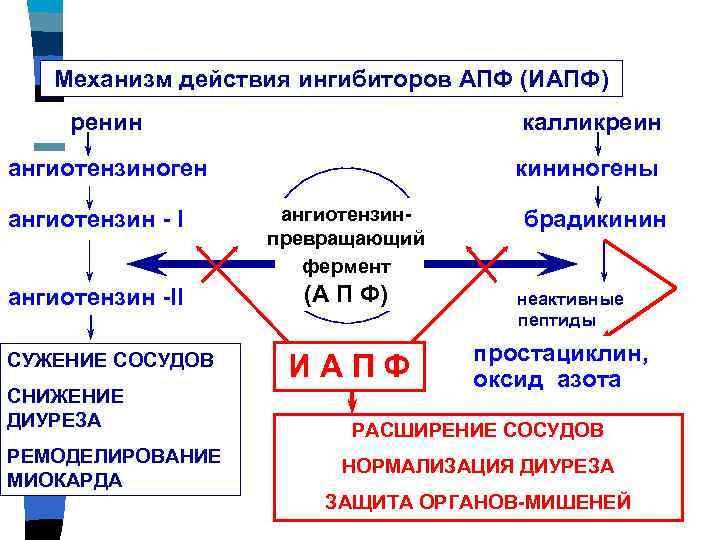
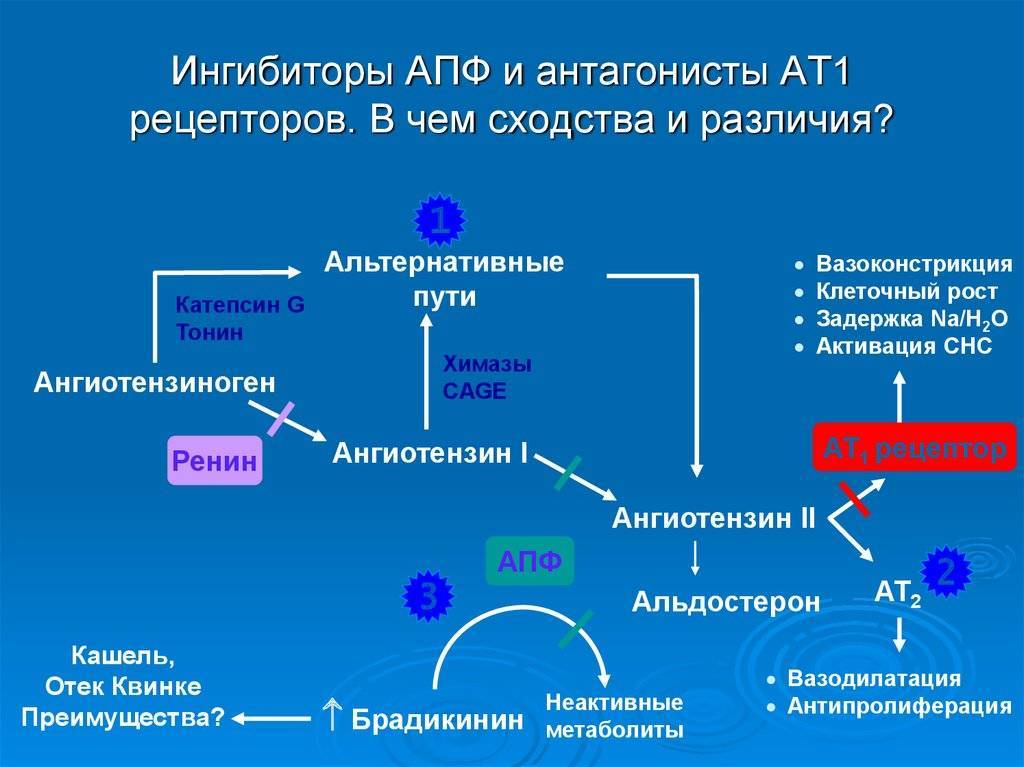
БРА отличаются хорошей переносимостью, в том числе и по сравнению с иАПФ, поскольку не вызывают кашель. Высокий профиль безопасности препаратов этой группы — залог приверженности больных лечению и успешного результата. Побочные эффекты, которые могут возникать при приеме сартанов, обычно мало выражены. Как правило, они носят преходящий характер и редко становятся основанием для отмены лечения.
О чем предупредить клиента?
На фоне приема сартанов очень редко возникают неблагоприятные реакции — по данным исследований, их частота такая же, как при приеме плацебо. Тем не менее зарегистрированы такие побочные эффекты, как головная боль, головокружение и общая слабость. Обычно они проходят сами и не требуют отмены препарата .
В заключение еще раз подчеркнем: иАПФ и БРА доказали и гипотензивный, и кардиопротективный эффект. Подавляющее большинство препаратов этих групп (за исключением фимасартана) сегодня применяется для лечения широкого спектра сердечно-сосудистых заболеваний
Единственное важное условие их эффективности — регулярный, длительный прием и соблюдение всех рекомендаций врача. Напомнив об этом посетителю с рецептом на иАПФ и БРА в конце консультации, первостольник выполнит свой профессиональный долг, приобретет лояльного клиента, а заодно внесет свой вклад в борьбу с одним из самых распространенных заболеваний в мире.
Источники
- Карабаева А. И. и др. Этиология, патогенез, клиническая картина артериальной гипертензии в пожилом возрасте //Вестник Казахского Национального медицинского университета, 2013. № 4.
- Saleem T. S. M., Bharani K., Gauthaman K. ACE inhibitors–angiotensin II receptor antagonists: A useful combination therapy for ischemic heart disease //Open access emergency medicine: OAEM. 2010; 2 (51).
- Abuissa H. et al. Angiotensin-converting enzyme inhibitors or angiotensin receptor blockers for prevention of type 2 diabetes: a meta-analysis of randomized clinical trials //Journal of the American College of Cardiology. 2005; 46 (5): 821–826.
- Кузнецов В. И., Стуров Н. В. Применение ингибиторов АПФ и блокаторов рецепторов ангиотензина II (сартанов) в общей врачебной практике //Земский врач, 2010. № 2.
- Васильева А. Д. Блокаторы ангиотензиновых рецепторов в лечении артериальной гипертонии //Русский медицинский журнал, 2007. Т. 15. № 23. С. 1–5.
- Linda L. Herman; Khalid Bashir. Angiotensin Converting Enzyme Inhibitors NCBI (дата обращения 31.07.2019). URL: https://www.ncbi.nlm.nih.gov/books/NBK431051/
- Осадчий К. К., Подзолков В. И. Сердечно сосудистый континуум: могут ли ингибиторы АПФ разорвать «порочный круг»? //Редакционная коллегия, 2008. С. 7.
- Несукай Е. Г. Зофеноприл: ингибитор ангиотензинпревращающего фермента с особыми свойствами //Український кардіологічний журнал, 2013. № 2. С. 97–102.
- Горбунов В. М. Спираприл – современный ингибитор ангиотензинпревращающего фермента //Кардиоваскулярная терапия и профилактика, 2005. Т. 4. № 3 ч I.
- Сычев Д. А.., Муслимова О. В. Органопротективные аспекты хинаприла: фармакогенетические аспекты //Кардиоваскулярная терапия и профилактика, 2011. Т. 10. № 2. С. 98–101.
- Сиренко Ю. Н. Эналаприл в кардиологии и терапии: стандарт эффективности и безопасности среди ингибиторов АПФ //Новости медицины и фармации, 2011. № 13–14. С. 6–8.
- Булдакова Н. Г. Антагонисты рецепторов ангиотензина в клинической практике //Рус. мед. журн., 2008. № 11. С. 1567–1570.
- Бронская Г. М., Коршак Т. А., Казакевич Д. В. Клинико-фармакологическая характеристика блокаторов рецепторов ангиотензина II в лечении артериальной гипертензии и хронической сердечной недостаточности //Проблемы здоровья и экологии, 2009. № 3 (21).
- Чазова A. Е. Возможности нового блокатора рецепторов к ангиотензину II азилсартана медоксомила в лечении артериальной гипертонии у пациентов с метаболическими нарушениями //Системные гипертензии, 2015. Т. 11. № 4. С. 58–61.
- По данным ГРЛС на 01.08.2019.
Препараты альфа-адреноблокаторов
К альфа-адреноблокаторам второго поколения относятся доксазозин и теразозин, к подгруппе третьего поколения относятся альфузозин и тамсулозин. Они рекомендованы урологическими ассоциациями (например, американской AUA, канадской CUA) в качестве вариантов лечения лиц с СНМП, вторичными по отношению к доброкачественной гиперплазии простаты. Альфа-блокаторы первого поколения и празозин не рекомендуются.
Механизм действия альфа-адреноблокаторов приводит к расслаблению гладкой мускулатуры как простаты, так и шейки мочевого пузыря, поскольку ингибируют симпатическую стимуляцию, опосредованную α-адренорецепторами.
α-адреноблокаторы второго и третьего поколения хорошо зарекомендовали себя при лечении симптомов нижних мочевых путей, возникающих из-за дисплазии. Несмотря на то, что есть небольшие различия в их побочных эффектах, они считаются одинаково клинически эффективными и обеспечивают наиболее быстрое облегчение симптомов.
- Плюсы их применения: альфа-адреноблокаторы действительно улучшают симптомы.
- Минусы применения: они не обеспечивают длительного снижения возможности острой задержки мочеиспускания и не отодвигают хирургическое вмешательство, связанное с заболеванием.
 Препараты альфа-адреноблокаторов
Препараты альфа-адреноблокаторов
Препараты третьего поколения тамсулозин и альфузозин, в отличие от альфа-адреноблокаторов второго поколения, не нуждаются в корректировке дозировки с течением времени. Считается, что они более эффективны. Они избирательно расслабляют гладкие мышцы простаты, следовательно, они не оказывают влияние на артериальное давление.
Основные нежелательные явления, о которых сообщалось при приеме альфа-адреноблокаторов, – ортостатическая гипотензия, головокружение, усталость (астения), проблемы с эякуляцией и заложенность носа. Риск головокружения ниже при приеме тамсулозина и альфузозина, чем при приеме препаратов второго поколения. Обнаружено, что тамсулозин имеет более низкую вероятность ортостатической гипотензии, но более высокую частоту эякуляторной дисфункции (10%). Он не вызывает эректильной дисфункции или снижения полового влечения.
Немного цифр
Немного статистики. В Великобритании назначается около 24 млн. НПВС в год. 70% лиц старше 70 лет принимают НПВС 1 раз в неделю, а 34% ежедневно. В США продается НПВС на сумму до 6 млрд. в год. Как следствие, риск развития желудочно-кишечных кровотечений (ЖКК) возрастает 3–5 раз, прободения — в 6 раз, риск смерти от осложнений до 8 раз. До 40–50% всех случаев острых ЖКК связаны с НПВС.
Проблема эта актуальна и в нашей стране, к примеру по данным Научного Центра сердечно-сосудистой хирургии им. А.Н. Бакулева из 240 больных, ежедневно принимающих аспирин даже в малых дозах, на гастроскопии поражения желудка и 12 п.к выявлены у 30% (из них язвы — у 23,6%, эрозии — у 76,4%). Аналогичная картина у коллег из ВНИИ ревматологии РАМН — у 2126 пациентов, принимающих НПВС без «прикрытия» (защиты) желудка, эрозии и язвы гастродуоденальной зоны найдены в 33,8% случаев. Это очень впечатляющие и драматические цифры осложнений от приема НПВС, учитывая количество употребляющих эти препараты людей в развитых странах.
«Волшебные» пилюли
Существует группа препаратов, под общим названием нестероидные противовоспалительные (НПВП), которые мы все хотя бы раз в жизни, а многие регулярно, принимали. Это препараты, обладающие обезболивающим противовоспалительным и / или жаропонижающим действием. В качестве примера можно назвать Аспирин, Нурофен, Найс, Кетанов, Кетопрофен и прочие. Учитывая «волшебные эффекты» от их действия — снятие воспаления, боли и жара, — их назначают практически все, всем и всегда. Назначают травматологи, ревматологи, терапевты, лоры, стоматологи. Плюс, их можно совершенно свободно приобрести в любой аптеке. Но, наряду с «волшебными свойствами» эти лекарства обладают рядом побочных действий, которые можно разделить на 2 группы: кардиориски и гастро риски. Собственно о гастрорисках и пойдёт речь в данной статье.
Препараты 5-ARIs или ингибиторов 5α-редуктаз
Дутастерид и финастерид, которые относятся к ингибиторам ферментов 5α-редуктаз, действуют, блокируя переход тестостерона в DHT или дигидротестостерон. DHT – андроген, который отвечает за увеличение предстательной железы.
Класс ингибиторов ферментов 5α-редуктаз представляет собой единственную в настоящее время фармакотерапию, которая демонстрирует как эффективность, так и приемлемую безопасность для медикаментозного лечения ДГПЖ. Продемонстрировано, что снижение DHT вызывает апоптоз и атрофию эпителиального эпителия простаты. Следовательно, обоснование использования 5-ARIs для терапии аденомы простаты заключается в снижении сывороточных и особенно клеточных уровней дигидротестостерона, приводя к уменьшению размера простаты.
Финастерид, который ингибирует изоферменты 5-AR (альфа-редуктазы) типа 2, подавляет сывороточный DHT на 70,8% ± 18,3% через 24 недели, но не до критических уровней.
Дутастерид обеспечивает более высокий уровень подавления сывороточного дигидротестостерона (95% ± 3%) и способен подавлять как 1-й, так и 2-й тип изоферментов 5-альфа-редуктаз. Согласно рекомендациям Американской и Канадской Урологических Ассоциаций, оба препарата подходят для применения при наличии симптомов нижних мочевыводящих путей, связанных с очевидным увеличением предстательной железы. Однако их не следует использовать, когда отсутствует увеличение простаты.
Проведено четырехлетний анализ долгосрочной эффективности, также безопасности применения препарата Проскар (Proscar, МНН финастерид). Установлено, что прием препаратов привел:
- к уменьшению размера/объема простаты на 18%. При использовании плацебо орган увеличился на 14% (p <0,0001);
- к улучшению оценки симптомов, оценка проводилась с использованием подсчета по баллам AUA-SI (2,6 балла против 1,0 для плацебо; p <0,001);
- и снизило по сравнению с плацебо риск ОЗМ на 51% и хирургического вмешательства на 55% (p <0,001 для обоих).
Применение финастерида в недавно опубликованной работе «Медицинская терапия простатических симптомов» (MTOPS) уменьшило величину простаты на 19%, но, что более важно, снизил риск клинического прогрессирования на 34% (до 2,9 на 100 человеко-лет) по сравнению с плацебо.
Препараты 5-ARIs или ингибиторов 5α-редуктаз
Применение дутастерида (исследование проводилось в течение двух лет) продемонстрировало снижение размеров предстательной железы примерно на 26%, которое сохранялось в течение дополнительных 2 лет. Лечение дутастеридом также сопровождалось улучшением симптоматики на 4,5 балла (против 2,3 балла для плацебо; p <0,001), снижением рисков ОЗМ на 57%, уменьшением хирургического вмешательства на 48%. Недавно опубликована исследовательская работа CombAT (лечение комбинацией аводарта и тамсулозина). Специалисты изучили и сравнили данные применения дутастерида, тамсулозина и их комбинированного приема в первые два года.
Впервые выяснилось, что в популяции пациентов с величиной простаты более 30 см3 и показателем ПСА> 1,5 нг/мл (оптимальная популяция для терапии 5-ARI) лечение ингибиторами 5α-редуктаз (а именно дутастеридом) привело к значительно большему уменьшению симптомов, чем альфа-блокатор тамсулозин.
Комбинированная терапия
Пациентам при наличии увеличенной предстательной железы с симптомами обструкции выходного отверстия мочевого пузыря рекомендовано лечение как ингибиторами 5α-редуктаз, так и альфа-адреноблокаторами. Обоснование этой рекомендации – быстрое облегчение симптомов альфа-адреноблокатором с одной стороны и более длительное облегчение симптомов с помощью 5-ARI с другой стороны
Что еще более важно, 5-ARI снизит риск серьезных осложнений, таких как острая задержка мочи и/или необходимость хирургического вмешательства по поводу аденомы простаты
В исследовании “медицинской терапии симптомов простаты” MTOPS риск прогрессирования при комбинированной терапии (финастерид и доксазозин) снизился на 66%. В дополнение к этому открытию, ученые установили, что потребность в хирургическом вмешательстве и риск ОЗМ были снижены при комбинированной терапии и при применении финастерида отдельно, но не при монотерапии доксазозином. Аналогичным образом исследование CombAT показало через 2 года, что уменьшение симптомов и беспокойства, а также вопрос 8 IPSS (качество жизни) были значительно выше при комбинированной терапии (дутастерид и тамсулозин), чем при любом режиме монотерапии.
Результаты исследования «Управление симптомами после сокращающей терапии» (SMART) и PROACT (комбинация Проскара и альфа-блокатора с последующим испытанием прекращения терапии) показывают, что для большинства пациентов альфа-блокатор можно безопасно отменить через 6–9 месяцев комбинированной терапии без снижения эффективности. Потенциальные преимущества отмены альфа-адреноблокатора включают более низкую стоимость, меньшее количество побочных эффектов и лучшее соблюдение режима лечения. Следовательно, если пациент хорошо себя чувствует на комбинированной терапии, целесообразно отменить альфа-блокаторы через полгода.
Варианты лечения аденомы предстательной железы, протекающей с симптомами мочевых путей
Варианты лечения включают:
- изменение образа жизни;
- ожидание, сопровождающееся динамическим наблюдением;
- фармакологические препараты;
- нехирургические процедуры;
- хирургические операции.
Лечение, будь то консервативное или более агрессивное, направлено на улучшение оттока мочи, облегчение симптомов, которые может испытывать человек, и задержку или предотвращение прогрессирования гиперплазии. Выбор тактики с точки зрения пациента может отличаться от выбора врача. Выбор правильного лечения лучше проводить не только исходя из личных предпочтений пациента, а совместно с рекомендациями уролога (у которого есть опыт и необходимые знания).
Каждый вариант лечения облегчит и улучшит симптомы, но каждый из них имеет различные риски, осложнения и шансы на успех
Крайне важно, чтобы предпочтения пациента в отношении конкретного лечения были сопоставлены с тяжестью симптомов и конкретными физиологическими переменными, используемыми при постановке диагноза урологом